
科技改变生活 · 科技引领未来

科技改变生活 · 科技引领未来
(报告出品方/作者:华创证券)一、能力完备、管线丰富,具备远大成长前景的优质药企苑东生物创立于2006年,是一家以研发创新为驱动,原料药制剂一体化的制药平台型企业。公司坚持“以患者为中心,为人类健康沐浴阳光”的企业使命,依托持续的技术创新,
(报告出品方/作者:华创证券)
一、能力完备、管线丰富,具备远大成长前景的优质药企
苑东生物创立于 2006 年,是一家以研发创新为驱动,原料药制剂一体化的制药平台型 企业。公司坚持“以患者为中心,为人类健康沐浴阳光”的企业使命,依托持续的技术 创新,逐步建立起国内领先、符合国际标准的研发技术及产业化平台,重点布局麻醉镇 痛领域,同时兼顾心血管、肿瘤、儿童用药、糖尿病等重大疾病领域,先后已实现了近 30 个化学药制剂产品和近 20 个化学原料药产品的产业化。
尽管从收入、利润、市值等指标来看,公司目前还都相对较小。但经过过去十余年公司 管理层和全体员工坚持不懈的努力,我们认为公司在制药企业尤其是化学药企业成长所 需的各项要素上均已积淀出过硬的能力。假以时日,公司有望沿着仿创结合的发展路线 不断成长,具备成为大中型、国际化制药企业的潜力。
管理层行业背景深厚,激励力度到位
公司董事长王颖女士拥有近 30 年医药行业从业经验。在其带领下,公司已组建起一支 极具国际化视野和业务专业度的管理团队。在高管层面,公司总经理袁明旭、总经理助 理纪昌平等均具备多年的医药行业从业经验。在技术骨干层面,公司的研发中心总经理 HONG CHEN 曾就职于美国强生露德清公司、美国 Teva 等药企,主持了 30 多个新药和 仿制药的研发,其中一个一类新药(Entereg)、15 个 ANDA 固体和液体制剂产品获得美 国 FDA 批准上市,具有丰富的新药研发经验和管理运营能力。其余技术骨干也多具备 海外或国内头部药企的任职背景。
在股权层面,董事长王颖女士直接及间接持有公司 43.55%的股权,为公司的实际控制 人。同时,公司核心管理人员及中层骨干也普遍通过楠苑投资(持股 5.71%)、榕苑投 资(持股 2.5%)、集合资产管理计划(持股 2.08%)和直接持股的形式拥有公司一定数 额的股权。良好的激励体系,有望为公司业务前景的持续兑现提供额外保障。
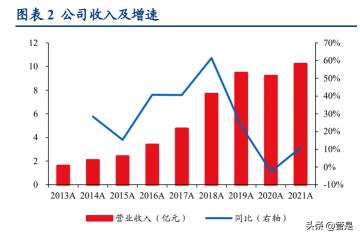
研发质量体系过硬,持续保持高强度投入
在研发和质量体系上,公司始终坚持高规格的研发投入和国际化的质量标准。根据公司 历年财报的披露,2013 年以来,公司研发费用率始终保持在 15%左右,2021 年前三季 度更是提升到接近 20%。在质量体系上,公司原料药基地已多次通过欧盟认证及美国、 日本多个客户的审计,同时无菌制剂生产线也是西南地区首家通过新版 GMP 认证。
依托于过硬的质量体系和持续较大的研发投入,公司目前已实现了近 30 个化学药制剂 产品和近 20 个化学原料药产品的产业化。已上市的制剂产品中有 6 个为国内首仿,半 数以上的品种均是国内前三家获批。在原料药产品中,也有近 10 个化学原料药产品已 出口国际市场。一系列数据,反映出无论是原料药还是制剂的环节,公司均已在国内化 学药企业中处于较为领先的水平。
仿创结合,在研管线非常丰富
综合 CDE 申报情况和公告等信息,可以看到经过过去多年持续的高强度研发投入,公 司已经积淀起一条非常丰富的仿创结合的研发管线。目前公司已披露的在研产品超过 30 个,其中仿制药项目超过 20 个,创新药项目超过 10 个。分品类来看,其中麻醉镇痛 产品在 10 个以上,心血管产品在 7 个以上,儿童药在 6 个以上,抗肿瘤等其他品种 7 个以上。
2019-2021 年,公司新产品的获批数量分别为 2、6 和 3 个。根据公司管线品种的申报时 间和获批周期推算,我们估计 2022-2024 年公司新获批产品数量存在进一步提速的潜力。
从短、中、长期的维度来看,若管线产品获批顺利,公司各类产品的落地和放量有望形 成接力,使得快速成长的趋势在未来较长周期中延续,并可能在 2023、2024 年前后结 合国际化和创新药的突破出现进一步的加速:
1)短期来看,公司存量品种的集采已基本落地,部分品种集采后仍具备较为明确的放 量潜力。每年 10 个左右新的增量仿制药品种的获批,有望给公司带来持续的增长拉动;
2)中期,国际化和精麻管制品种若顺利兑现,有望打开公司成长天花板,并可能在业 绩端带来进一步的提速;
3)远期,创新药产品的陆续落地有望与公司高端仿制药品种和国际化品种形成接力, 拉动公司业绩在更长周期中实现快速成长。(报告来源:未来智库)
二、原料药制剂一体化产品国内批量上市,支撑短中期业绩快速增长
公司目前的收入和利润主要由近 30 个已获批的国内仿制药产品来贡献,占到公司收入 的 90%左右。剩下的 10%由原料药和技术服务两块业务贡献。
根据上海阳光采购网披露的第七批的集采目录,公司将有 5 个品种参与第七轮集采(2 个存量、3 个增量)。而经过这一轮集采后,公司现有规模较大品种将基本完成集采。展 望未来,我们认为一方面公司部分存量品种仍具备着一定的放量潜力;另一方面也更为 重要的是,后续管线中大量新品种的获批和集采中标,有望带来源源不断的新的增长动力。综合以上两点,我们认为短中期内公司业绩仍具备快速增长的潜力。
(一)存量品种集采即将基本落定,部分品种仍具备一定的放量潜力
根据招股书的披露,2019 年富马酸比索洛尔片、伊班膦酸钠注射液、乌苯美司胶囊、注 射用复方甘草酸苷、盐酸纳美芬注射液、枸橼酸咖啡因注射液、布洛芬注射液等七个制 剂品种的收入占据了公司制剂总收入的 95%。根据中康数据及公司公告的披露,我们估 计这 7 个品种在公司目前的收入中仍占有较大的比重。
通过对这七个品种的具体分析,我们认为随着国家第七批集采的落地,公司存量品种的 竞争格局将基本稳固。未来依托于终端用量的进一步增长、院内院外渠道的开拓,部分 品种依然具备较为明确的成长前景,具体来看:
1)富马酸比索洛尔片和布洛芬注射液两个品种均已集采完毕。其中富马酸比索洛尔片 在 2020 年 1 月的第二轮集采中第一顺位中标。根据中康数据,公司这一品种在集采后 市占率增长较快。未来随着院内和院外市场市占率的进一步提升,我们预计该品种 2022 年起仍有望实现较为可观的增长。
而另一品种布洛芬注射液虽然在 2021 年 2 月的第四批集采中丢标,但该品种在 2018 年 才由公司在国内首家实现上市,推广时间较短,目前全国的绝对用量和入院率均处于较 低的水平。考虑到布洛芬注射液疗效明确且 2021 年新进全国医保,我们预计品种本身还存在着较大的放量潜力。公司该品种在 2021 年消化了集采未中标的压力后,从 2022 年起在低基数下仍有望实现较好的增长。
2)伊班膦酸钠注射液和枸橼酸咖啡因注射液即将参与今年的第七批集采。根据中康数 据,2021 年前三季度公司这两个品种的市占率分别为 39%和 24%。
目前这两个品种分别是 4 进 3 和 7 进 5 的竞争格局。由于参与竞争企业相对较少,只要 公司能够实现中标,我们认为份额的压力相对较小。同时,考虑到集采后企业的销售费 用通常会有较明显的下降,若不出现极端的价格降幅,我们预计这两个品种的利润仍有 望维持。
3)注射用复方甘草酸苷、盐酸纳美芬注射液目前均无厂家通过一致性评价,我们认为 可能是由于生产技术壁垒较高所致。乌苯美司胶囊也于 2019 年被移出医保目录,大概 率不会出现在集采的目录中。综上,这三个品种我们认为在较长时间内预计将不受到集 采的影响,处于较为稳定的状态。
(二)增量品种批量化上市,为公司业绩持续快速增长提供充足保障
除招股书披露的 7 个主要制剂产品外,我们认为更值得关注的是 2019 年以来公司不断 获批新品种的能力。源源不断的新品种获批,也正在给公司带来越来越显著的业绩增量。
基于 2018 年之后国内仿制药市场的特征,我们认为公司这些增量品种是否还有机会参 与集采以及集采中标与否,将会是决定这部分品种未来放量的关键因素。所以根据这些 品种的集采情况,我们将公司近年来获批的增量品种分为已参与集采并中标,即将参与 集采和其他三个类别。
已集采增量品种
从第三批集采开始,增量品种给公司业绩的拉动力已开始逐步体现,在第三到第五批的 集采中,公司已累计有 5 个品种实现中标。除了依托考昔片是 2020 年 8 月参与的第三 批集采,收入和利润增量在 2021 年已有部分体现外,注射用帕瑞昔布钠、达比加群酯 胶囊、盐酸法舒地尔注射液、格隆溴铵注射液均是 2021 年参与集采并中标。我们预计 2022 年这些品种的放量仍能够为公司业绩带来较大的拉动力。
以依托考昔为例,根据中康数据,集采之后公司的依托考昔院内市场的市占率从 2020 年的 2.97%快速上升至 2021 年前三季度的 34.38%。根据中康的市场规模及公司集采中 标价推断,我们预计 2021 年公司的依托考昔单品种的收入增量有望接近 5000 万元。
而公司 2021 年集采中标的 4 个品种中,帕瑞昔布钠和达比加群酯集采前(2020 年)的 销售量分别为 3100 万瓶和 770 万盒,销售额分别达 23.87 和 13.51 亿元。即便按照集采 后的价格计算,我们预计这两个品种也有望给公司带来较为可观的收入和利润增量。
即将参与集采品种
根据官方公布的第七批集采报量文件,我们认为公司的盐酸美金刚缓释胶囊、帕立骨化 醇注射液、富马酸丙酚替诺福韦片三个增量品种均有望参与第七批集采,一旦实现中标, 也有望在今明两年给公司带来显著的收入和利润增量。
从竞争情况来看,这三个品种中盐酸美金刚和帕立骨化醇格局较好,目前分别是 6 进 4 和 4 进 3 的状态。根据中康数据,这两个品种 2020 年的市场规模分别为 6.69 和 3.37 亿 元,同比增速分别达到 19%和 74%。尤其是帕立骨化醇注射液,2021 年前三季度增速 进一步加速至 168%,前三季度市场规模已达到 5.73 亿元。一旦公司能够在这两个品种 上顺利中标,有望为公司带来较为可观的收入和利润增量。
在研品种
除了上述已获批的产品外,2021 年的中报中公司还披露了 20 多个正在研发的高端仿制 药品种。根据这些品种的研发申报周期推断,我们预计未来几年公司每年新获批的产品 数量有望进一步加速。
从公开数据中公司已申报产品的进度来看,我们预计舒更葡糖钠注射液、盐酸去氧肾上 腺素注射液、丙戊酸钠注射用浓溶液、布瑞哌唑片、布洛芬氨丁三醇注射液、氨己烯酸 散、盐酸帕洛诺司琼注射液、盐酸尼卡地平注射液、艾司奥美拉唑镁肠溶干混悬剂、盐 酸阿罗洛尔片、注射用尼可地尔、盐酸纳布啡注射液、甲硫酸新斯的明注射液等品种均 有望在 2022 年和 2023 年陆续获批。
从 CDE 国内企业申报情况来看,上述品种中许多仍有望延续公司过去以前三家身位获 批的领先优势,且普遍具备原料药自给的能力。我们认为这些品种普遍具备较强的市场 竞争力,有望为公司带来持续的业绩拉动。(报告来源:未来智库)
三、制剂国际化和国内麻醉镇痛线蓄势待发,打开中期成长天花板
(一)制剂国际化:差异化布局潜力大品种,23 年起有望进入收获期
制剂的国际化,是公司中期战略中极为重要的一环。为了确保国际化的顺利推进,公司 已构建了国际顶尖的管理队伍,覆盖研发、FDA 注册、生产全产业链。其中核心技术领 军科学家 8 人大多具有丰富国际 MNC 大型药企研发与管理任职经历,被省市两级组织 部认定为“顶尖创新团队”。
公司的制剂国际化战略由子公司硕德药业实施。根据公司相关公告的披露,目前公司总 投资 6.2 亿元在硕德药业建设的符合 FDA cGMP 及欧盟 EU GMP 标准建立的重大疾病领 域创新药物系列产品产业化基地的建设一期工程各项单体均已完成。二期计划投资 3.36 亿元建设的的高端口服液车间、高活性高毒性注射剂车间及高端固体制剂车间也已在建 设过程当中。
而在 2021 年的半年报中,公司也对制剂国际化的最新情况进行了陈述:“公司按照“国 外短缺品种+自有原料药”的思路,已布局 5 个 ANDA 高端制剂品种,其中麻醉镇痛领 域的 EP-0084I 项目已经获得 FDA 的 CGT,正在硕德药业国际化基地开展国际化生产车 间中试,预计 2022 完成申报。API 国际化方面,完成了枸橼酸马罗匹坦的美国注册文件 递交,其他国际化研发项目正在按计划推进,原料药的研发产品管线得到进一步充实。”
EP-0084I 项目
结合“自有原料药”、“CGT”等线索分析,我们估计 EP-0084I 项目大概率应为纳美芬 注射液的 ANDA 申报。作为公司国际化的起点,该品种是重要的试金石,同时品种本 身也具备着较好的盈利前景。
所谓 CGT 资格,是 2017 年 FDA 为了进一步降低药价,减轻医保负担,专门针对专利 已到期但市场仍短缺的品种设计的仿制药鼓励政策。其具体要求为:1)已专利到期但 市场仅有 0 家或 1 家企业的品种;2)这一品种具备临床的必要性。2020 年 3 月,针对 CGT 的申请和审评过程中具体要求,FDA 颁布了《Competitive Generic Therapies Guidance for Industry》指南,进一步明确了申请人应该遵循的申请流程以及将药物指定 为 CGT 的标准。并明确了 FDA 如何为提交 CGT 的 ANDA 申请人提供加速审批支持和 有条件授予 180 天独占期奖励。
纳美芬正是一种典型的符合美国 CGT 标准的药物。其作用机理为阻止吗啡和阿片类物 质与人体阿片受体的结合,主要用于逆转阿片中毒以及治疗酒精成瘾。
1995 年 4 月,盐酸纳美芬注射液获得美国 FDA 批准上市。2009 年,纳美芬 NDA 的持 有人 Baxter Healthcare Corporation 通知 FDA,由于商业原因,0.1mg base/mL 和 1.0 mg base/mL 的 REVEX(盐酸纳美芬注射液)的生产和销售已于 2008 年 5 月 21 日停止并在美 国退市。但 2008 年、2013 年、2019 年,纳美芬先后获得了中国、欧盟、日本相关部门 的批准,开始在这些国家上市销售。在 2017 年 FDA 公开的文件当中,也明确表示了纳 美芬注射液在美国是由于商业原因退市,而不是安全性和有效性的因素。
2022 年 2 月 8 日,Purdue 的盐酸纳美芬注射液通过 CGT 的通道正式获批,用于已知或 疑似阿片类药物过量使用的紧急治疗,成为目前美国市场唯一上市的纳美芬产品。目前 终端仍处于非常好的竞争格局。
逆转阿片中毒药物在美国市场拥有较大的终端需求。根据 NCDAS(National Center for Dryg Abuse Statistics)的统计数据显示,目前美国 12 岁以上的非法吸毒人群已达 3190 万人,占人群总数的 11.7%。其中使用阿片类药物的吸毒者占美国总吸毒人群的 36%。
过去十余年中,纳美芬退市后美国市场承担相关治疗需求的主要药物为纳洛酮。彭博数 据库显示,目前美国市场纳洛酮销售规模在 5 亿美金左右。考虑到药店和医院以外的渠 道未被统计在内,我们估计实际市场规模可能比这一金额更大。 美国吸毒人群总人口占比 纳洛酮美国市场销售额(亿
事实上,从临床数据来看,我们认为针对已知或疑似阿片类药物过量使用的紧急治疗, 纳美芬相较纳洛酮效果更优。与纳洛酮相比,纳美芬拥有更长的半衰期(纳洛酮的 4 倍 以上)和更好的生物利用度。临床数据表明,纳美芬在逆转急性阿片类药物过量相关的 呼吸抑制时,作用持续时间更长,且副作用相对较少。疗效上的优势,使得纳美芬在美 国上市后有望对纳洛酮形成有力替代。
就审批周期而言,GDUFA 法案执行后,近年来仿制药的获批周期通常在 10 个月-2 年之 间。而 CGT 品种由于享受加速通道,在产品申报资料和企业质量体系不存在重大瑕疵 的情况下,审批周期有望进一步缩短到 8 个月。
根据公司 2021 年半年报的披露,公司的纳美芬注射液将在 2022 年底之前完成注册申报。 以此推算,我们预计公司产品在 2023 年年内获批的概率较大。由于公司拥有原料药制 剂一体化和国内生产效率的优势,一旦成功上市,或将拥有比 Purdue 更强的竞争力, 为公司带来较为丰厚的收入和利润回报。
以纳美芬为突破口,我们预计公司有望从 2023 年开始逐步迎来制剂国际化的收获期。 根据公司相关公告的表述:“公司以国外市场紧缺、专利期长、用药周期长以及首仿抢 仿 PIV 申报的思路去布局国际化在研管线,目前已储备 5 个国际化高端注射剂和口服制 剂,预计在 2022 年底前完成注册申报,2023 年有 2 个 ANDA,2024 年有 3 个 ANDA 获批,并且未来每年有 3 个新增立项。”未来随着每年几个 ANDA 品种的获批,制剂出 口业务也有望成为公司业绩的重要驱动因素。
(二)麻醉镇痛:仿创结合,伴随品种持续落地有望成为该领域国内领先企业
国内产品方面,麻醉镇痛用药是公司发力的重点。麻醉镇痛用药由于强管控和临床刚需 的特点,在药品各适应症领域中市场空间、竞争格局等均处于较好的状态。
公司基于对麻醉镇痛领域疾病机理的深入研究,按照“全细分领域、全作用机制、全镇 痛模式、全业务领域”的策略思路,已构建起国内企业最为丰富的麻醉镇痛管线之一。 目前,已上市品种达到 9 个,在研品种达到 20 余个。未来随着后续产品的落地,公司 在收入利润持续增厚的同时,有望向这一领域的国内领先企业迈进。
1、管控严格,精麻类药物拥有较高的进入门槛和较好的竞争格局
由于精麻药的特殊属性,国家将精神麻醉类药品分为麻醉药品、第一类和第二类精神药 品进行严格管制。采取定点生产制度且限制生产厂家数量,政府实行统一定价,存在较 高的政策壁垒。
根据《麻醉药品和精神药品管理条例》规定,麻醉药品及精神药品的原料药和制剂的定 点生产企业数量有明确限制。对麻醉和精神类药品实施分级管理,即便是管制级别最低 的二类精神药品,生产同一品种的原料药企业最多也只能有 5 家,制剂企业最多只能有 10 家。这一政策壁垒的存在,为相关生产企业提供了较好的竞争格局。
2、市场规模巨大且保持快速增长
根据中康数据,我们将镇痛药、麻醉药、催眠镇静药、抗震颤麻醉药和肌肉松弛用药五 个主要精麻类药物品种的销售额进行汇总,我们预计 2021 年我国等级医院精麻类药物 市场规模已经接近 500 亿元。
过去,受“限手术麻醉”制度的限制,部分麻醉药物仅能在手术当中进行使用。这也使得 临床手术量与麻醉药物的用量呈显著的正相关性。根据中国卫生健康统计年鉴的数据, 近年来我国临床手术人次始终保持 10%以上的持续增长,2019 年我国医疗机构住院病 人手术人次达到 6930 万人次。
2018 年 8 月,国家卫健委发布《关于印发加强和完善麻醉医疗服务意见的通知》。通知 指出,相关机构要加强手术室外麻醉与镇痛,优先发展无痛胃肠镜、无痛纤维支气管镜 等诊疗操作和分娩镇痛、无痛康复治疗的麻醉,通过医联体将疼痛管理向基层医疗卫生 机构延伸,探索居家疼痛管理新模式。
我们认为,随着疼痛管理型概念的逐步普及,部分麻醉药品取消“限手术麻醉”的限制, 我国精麻药物的应用场景有望得到极大的拓宽。疼痛管理新模式下精麻药品的需求增量 与不断增长的手术用量相叠加,我国精麻药物的市场规模有望在未来较长的周期实现持 续的增长。
3、公司精麻品种丰富,管制类特药及创新药陆续获批有望拉动公司业绩进一步加速
根据公司 2021 年中报的披露,公司目前已上市麻醉镇痛及相关领域产品 9 个,在研 20 余个,其中新药 5 个、管制类特药 9 个,逐步树立苑东麻醉镇痛品牌地位。从已经可以 在 CDE 官网看到申报信息的品种来看,甲硫酸新斯的明注射液、盐酸纳布啡注射液、 舒更葡糖钠注射液等品种均具有较大的市场规模和良好的竞争格局。
我们认为,由于我国精麻药物市场拥有较高的行政壁垒和广阔的用药人群。公司管制类 精麻药物一旦成功获批,将有望面对较好的竞争格局并在较短中期中实现快速放量。未 来随着公司这些新的麻醉品种从今年开始起成梯队上市,精麻类产品有望成为公司中长 期业绩持续快速增长的主要拉动力之一。
四、创新升级保持高强度投入,预计 2025 年前后进入收获期
在创新升级的道路上,公司也一直保持着高强度的投入,立项了多个差异化的创新药品 种。根据公司年报和招股书的披露,公司已有 10 余个 1 类创新药在研,创新管线涵盖 精麻、糖尿病、心血管、肿瘤等多个领域,其中已经/即将开展临床实验的有 3 个,进 度最快的优格列汀片已进入 III 期临床。我们预计从 2025 年开始,公司有望进入自主创 新药的收获期,沿着产业价值链实现进一步的飞跃。
优格列汀
优格列汀是公司目前创新药管线中进度最快的品种。其作用机理为长效二肽基肽酶-IV (DPP-4)抑制剂,已于 2022 年 2 月完成了首例临床 III 期试验的病人入组,或将成为 国内首款上市的长效口服降糖药物。
根据公司公告披露的 II 期数据,优格列汀片在每周给药 1 次、给药 12 周后,各剂量组 均可有效控制患者糖化血红蛋白,降低患者空腹及餐后血糖,400mg 组的降糖效果不弱 于目前口服降糖药中降糖效果最好的 SGLT-2。在安全性方面,各剂量组不良事件的发 生率与安慰剂组相比,差异无统计学意义,安全性良好。
根据中康数据和公司招股书的披露,目前国内口服降糖药市场规模约在 300 亿元,且仍 保持较快的增长状态。其中降糖效果较好的 SGLT-2 产品达格列净 2021 年的销售额已突 破 25 亿元,同比增长 140%以上。我们认为,公司的优格列汀具备不弱于 SGLT-2 的口 服降糖效果,且和一天服药一次的其他口服降糖药物相比,一周一次的用药模式具有更 好的依从性。一旦成功实现上市,有望给公司带来的较大的收入和利润弹性。
五、看好公司成长潜力
我们认为尽管从收入、利润、市值等指标来看,公司目前还都相对较小。但经过过去十 余年公司管理层和全体员工坚持不懈的努力,我们认为公司在制药企业尤其是化学药企 成长所需的各项要素上,均已积淀出了较为过硬的能力。假以时日,公司有望沿着仿创 结合的发展路线不断向中大型国际化制药企业迈进,具备远大的成长前景。从业务细节 上看:
1)短期来看,公司存量品种的集采已基本落地,部分品种集采后仍具备较为明确的放 量潜力。每年 10 个左右新的增量仿制药品种的获批,有望给公司带来持续的增长拉动;
2)中期,国际化和精麻管制品种若顺利兑现,有望打开公司成长天花板,并可能在业 绩端带来进一步的提速;
3)远期,创新药产品的陆续落地有望与公司高端仿制药品种和国际化品种形成接力, 拉动公司业绩在更长周期中实现快速成长。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)
精选报告来源:【未来智库】。

马龙东
